Beräkning av mäsk-pH

Mäskens pH-värde kommer att landa där alkalinitet och aciditet möts, där positiva och negativa laddningar balanseras. En brist kring det ursprungliga resonemanget om RA i del I är det inte tar hänsyn till vattnets verkliga pH och mäskens målvärde. Detta har nämligen påverkan på laddningar och buffertförmåga. Alkalinitet, enligt den ursprungliga definitionen, är ett mått på buffertkapacitet men riktar sig alltså mot pH 4.3 och det är inte där man vill ha sin mäsk. För att kunna förutsäga var mäsk-pH:t ska landa måste målet vara känt. Uträkning sker enligt formeln nedan, där hänsyn tas till såväl buffertkapacitet, maltens egen-pH och förhållande mellan malt och vatten.
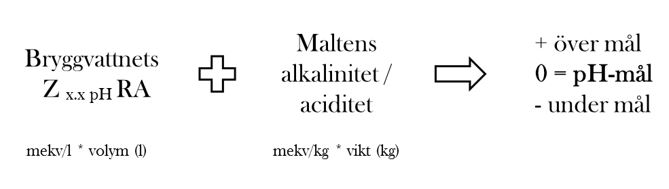
Z kommer ifrån tyskans ”ziel” som betyder mål och uträkningen är densamma som för RA, fast med skillnaden att Z-alkalinitet används istället för vattnets ursprungliga alkalinitet. Uträkning sker enligt nedan och mitt fall har jag valt ett målvärde på pH 5.2 för mäsken.

Antalet millimolekyler av karbonater i vattnet (Ct) räknas ut enligt följande.

Delta-C ovan är lika med skillnaden i laddning mellan pH 4.3 och vattnets ursprungsvärde. Information om aktuell laddning har jag hämtat ifrån en graf på s. 96 i boken Water, men det går troligtvis att få fram detta via andra källor också. Vid pH 8.3, som är värdet på mitt kranvatten, är laddningen -0,99 och vid 4.3 är denna -0,01. Varför delta C i mitt fall är lika med +0,98 ((-0,01) – (-0,99)). Ett positivt tal eftersom det representerar alkalinitet. Ct är därför lika med vattnets alkalinitet, 1,639 dividerat med differensen i laddning 0,98 som blir 1,672 mmol/l.
Delta Cz ovan utgörs av skillnaden i laddning mellan mål-pH och vattnets ursprungliga laddning. Vid pH 5.2 är laddningen -0,06 och följaktligen blir delta Cz 0,93 mekv/mmol i mitt fall ((-0,06) – (-0,99)). Mitt vattens nya alkalinitet, vid målet 5.2 mäsk-pH, blir således 1,672 * 0,93 = 1,555 mekv/l och ett Z RA på ~1,11 mekv/l enligt nedan.
1,555 – ( ((30/20)/3,5) + ((1,5/12,1)/7) )
Så långt förhållandevis okomplicerat, värre är det avseende maltens bidrag. Maltens alkalinitet respektive aciditet erhålles enligt följande formel. Ett positivt värde innebär alkalinitet och ett negativt aciditet.

Där pH-End är detsamma som målvärdet för mäsken och pH-DI är maltens värde i destillerat eller avjoniserat vatten (de-ionoized). Buffertkapaciteten erhålles genom titrering. En teknik där en lösning tillreds i destillerat i vatten, därefter tillsätts ett visst mått av syra eller bas (mekv/l) och ett nytt pH-värde antecknas. Detta upprepas till en analyskurva kan skapas. Därefter deriveras kurvan som en funktion av pH-värdet och buffertkapaciteten vid varje pH-värde går att utläsa. Här faller mitt experiment eftersom jag inte har några värden buffertkapaciteten hos den malt jag använder. Tills jag har tagit reda på denna, fått tag på destillerat vatten och titrerat min malt, eller mäsk blir den återstående framställningen i viss mån en uppskattning. Den data som jag har tillgå är baserad på Weyermanns pilsnermalt och Briess Caramel 80 L. Vid pH 5.2 har pilsnermalten en alkalininitet på 20 mekv/kg, vid 5.3 15, vid 5.4 10 och vid 5.5 5 mekv/kg. Karamellmalten är sur och bidraget är negativt vid de aktuella nivåerna. Vid 5.2 är aciditeten -35 mekv/kg, vid 5.3 -40, vid 5.4 -45 och slutligen -55 mekv/kg vid pH 5.5.
Test av formelns giltighet
Vid min senaste lagerbryggning landade mitt pH på 5.5. I receptet stod 10 kg pilsnermalt och 260 gram karamellmalt till 36 l mäskvatten. Den justerade vattenprofilen låg på 67 ppm CaCO3, 120 ppm kalcium och ~2 ppm magnesium. Adderat till vattnet var dessutom 1 ml 80% mjölksyra.
Enligt formeln ovan förändras delta Cz till 0,87 mekv/mmol eftersom laddningen vid 5.5 är -0,12. Det ger en ny Z alkalintet på 1,13 mekv/l ((67/50)*0,87) och med hänsyn tagen till kalcium och magnesium en Z RA på -0,6 mekv/l. Multiplicerat med mängden vatten, 36 l, ger detta ett vattenbidrag om -21,6 enligt formeln ovan.
Pilsnermalten har en alkalinitet på 5 mekv/kg vid pH 5.5 och receptet innehöll 10 kg, vilket gör pilsnermaltens bidrag till 50. Karamellmalten är även här sur i detta avseende och har ett bidrag om -55 mekv/kg vid det aktuella pH-värdet och minskar således maltbidraget med -14,3 (-55*0,26). Det leder till följande.
-21,6 (vatten) + +50 (pilsnermalt) + -14,3 (karamellmalt) = ~14
I min mening ser det faktiskt ganska lovande ut. Enligt formeln skulle jag ha landat på 0, men det finns en del felkällor som har en viss betydelse. Min pH-mätare visar för det första endast hela tiondelar och mätresultat kunde lika gärna ha varit 5.54. Dessutom, och viktigast, så har jag inte riktiga värden för maltens buffertkapacitet och därmed dess alkalinitet/aciditet än. Slutligen finns det en tioprocentig felmarginal i min vattenrapport för aktuella värden.
Formeln äger således viss giltighet varför det lämpar sig att återgå till det ursprungliga fallet med ett målvärde om pH 5.2, mitt vatten och normala maltnota. I detta läge har mitt vatten en Z RA på 1,11 mekv/l. Med utgångspunkt i det verkliga exemplet ovan för en ordinär lager ligger jag vanligtvis på ungefär 2,5% karamellmalt och 97,5% pilsnermalt, med en ratio på 3,6 l / kg. 10 kg pilsnermalt ger, vid pH 5.2, ett bidrag av 200 (20 mekv/kg * 10 kg) och 250 gram karamellmalt reducerar bidraget med blygsamma -8,75 (0,25 * -35 mekv/kg). Maltbidraget totalt sett således ~190, och 36 liter vatten också ett positivt bidrag med ~40. Sammantaget överskrids målet följaktligen med 230 och en mäsk enligt vad som sagts bör följaktligen vida överskriva pH 5.2. Intressant vore förstås att veta med hur mycket, och var den istället skulle landa. Är det möjligt kasta om formeln och dra analogier till resonemanget som har förts av Kolbach och Palmer i del I angående pH-sänkning?
Enligt palmer kan man som sagt sänka mäskens pH med 0.1 genom att minska RA enligt 200/Rv, uttryck i ppm CaCO3. I mitt fall skulle det motsvaras av 55,56 ppm CaCO3 och det blir detsamma som en minskning av RA med ~1,1 mekv/l per 0,1 pH. För att landa på pH 5.2 hade mitt vattens Z RA behövt vara -5,3 mekv/l enligt formeln bakvänt, det vill säga genom att maltens bidrag divideras med vattenvolymen. Det är differens på 6,4 mekv/l (1,11- -5,3) och 6,4/1,1 är lika med 5,7 som får multipliceras igen med 0,1 (pH-ändringen per mekv). Det blir 57 hundradelar, ungefär 0.6 och innebär att mitt pH i så fall skulle landa på 5.8 med ett helt obehandlat vatten.
Jag tillredde en minimäsk i skala 1:100, med 97,5 g pilsnermalt, 2,5 g karamellmalt och 3,6 dl vatten för finna svar på frågeställningen ovan. Härvid passade jag också på att tillsätta syra (se vidare i del III) i syfte att ta reda på vid vilket RA mäsken landar på respektive pH-värde.



Bortsett från nummer ett ovan så tillsatte jag 3,6 ml 0,1 N-lösning av mjölksyra (del III), lät den lösas under några minuter innan varje ny mätning. Även om testen de facto verkar stämma hyfsat bra drog jag en del lärdomar av detta experiment, framförallt hänförliga till min metod. För det första gick pH-mätarens termometer endast till 60 grader och det var denna jag hade tänkt förlita mig på vid mätningarna. Självklart borde jag ha tagit reda på det i förhand. Inledningsvis mätte jag i kastrullen, där temperaturen låg på cirka 65 grader men övergick därefter till att ta ut ett mindre prov för mätning i ett glas. Jag förde sedan tillbaka provet. Metodfelet är tydligast vid den tredje mätningen, där ett temperaturfall ägde rum som dock inte registrerades till fullo vid pH-mätningen. Dessutom uppstod svårigheter i precisionsavseende vid nedskalning i så hög grad. Det kändes som att jag brast lite i precisionen vid uppmätning av malt och vatten. Än tydligare blir det i del III och ett annat test som genomfördes. Sammantaget är emellertid trenden ganska tydlig och överensstämmer någorlunda med hypotesen ovan, kanske i än högre grad om man bortser från bristerna i metoden.
I den tredje och sista delen kommer jag att gå närmare in på vilka åtgärder som kan vidtas för att träffa ett önskat målvärde för mäskens pH.

En reaktion till “Kontrollera mäskens pH-värde – Del II: Beräkning av pH”